Профессор кафедры экспериментальной медицины CIRM (на фото ниже в клинике в центре) Юрий Захаров для того, чтобы показать эффективность и безопасность предлагаемых им методов систематически проводит трансплантацию стволовых клеток себе уже более двадцати лет, см. ссылку на видео (в РФ ресурс может быть ограничен):
youtu.be/DXoVjNUPw4o?si=vKOcBo9JJnSz3eku
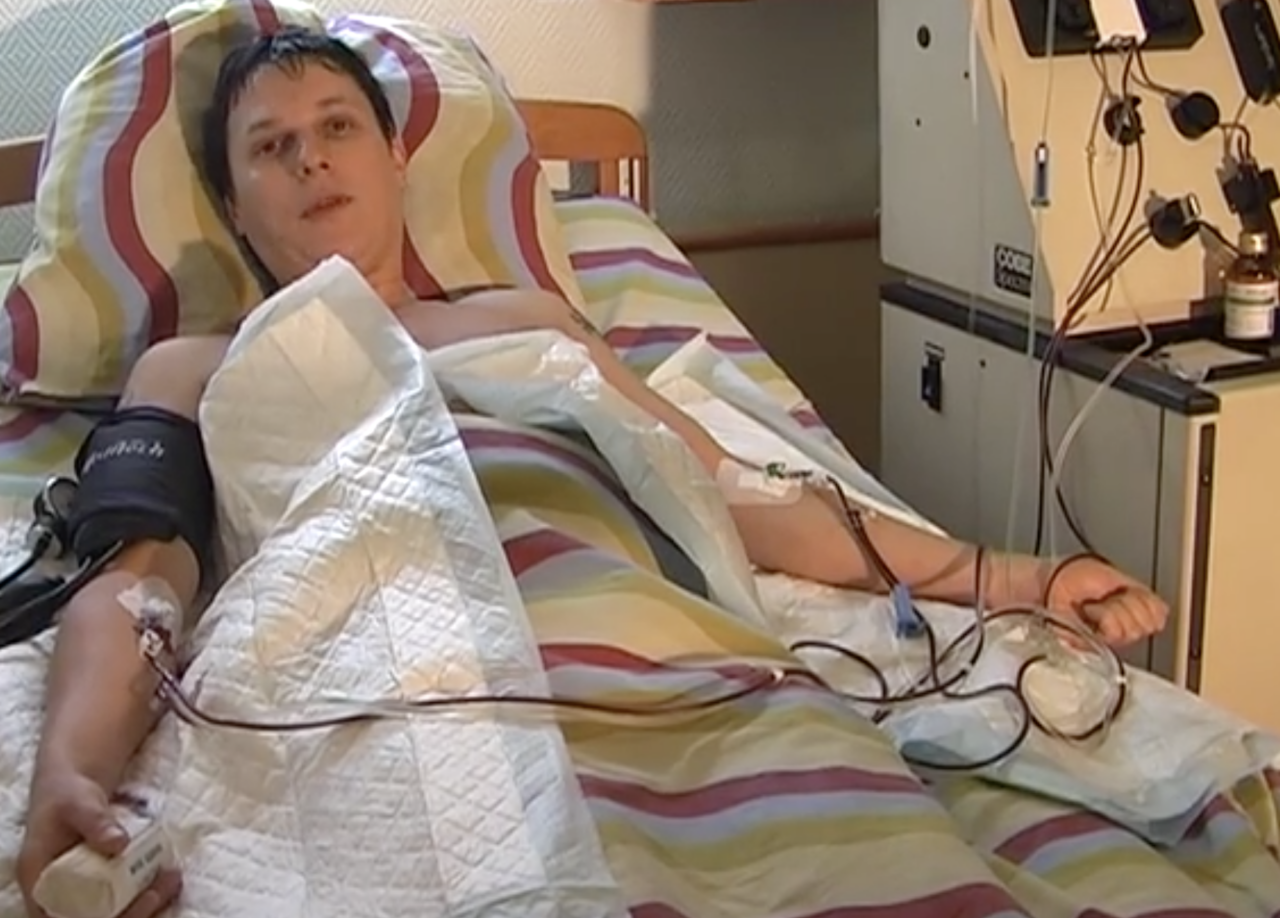
На апрель 2026 года мы проводим терапию сахарного диабета 1 типа аутологичными (вашими собственными после определенных манипуляций в лаборатории) гемопоэтическими стволовыми клетками и сертифицированными безопасными донорскими стволовыми клетками пуповины раннего прохождения (UC-MSC), произведенные в соответствии со стандартами клинического уровня. Для разных возрастных групп пациентов (до 18 лет и старше) используются разные технологии.

Мы используем технологию персонифицированной терапии клеточным препаратом на основе аллогенных стволовых клеток подобную Zimislecel, но она более безопасна — за пять лет применения побочных эффектов не установлено в отличие от фиксированных летальных исходов фазы 1/2 клинических испытаний Зимисцел.
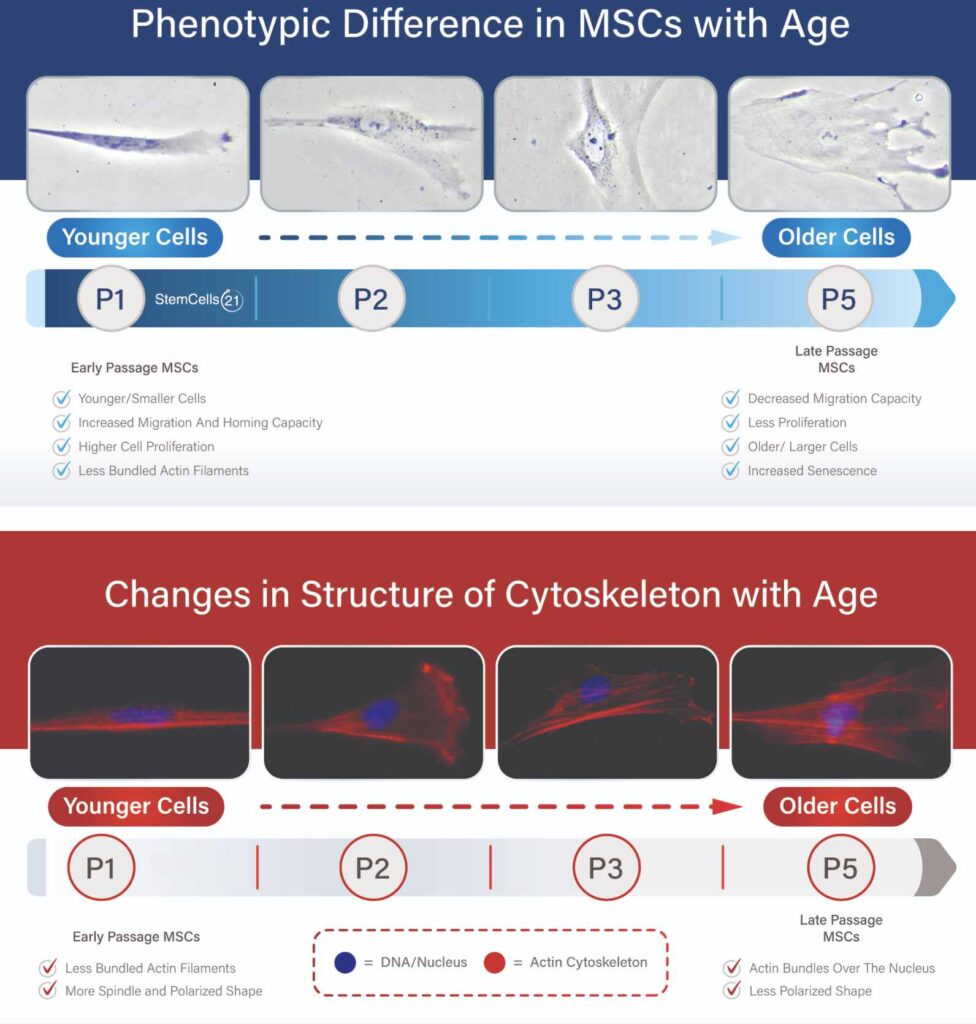
У данного типа стволовых клеток низкий уровень белков MHC класса II и других костимулирующих молекул, что позволяет им избежать отторжения при трансплантации. Это свойство позволяет проводить аллогенные трансплантации (от доноров), не опасаясь иммунного отторжения. Для терапии сахарного диабета 1 типа используются как ГСК, так и стволовые клетки пуповины раннего прохождения (UC-MSC), произведенные в соответствии со стандартами клинического уровня.
БЕЗОПАСНОСТЬ
Доказано — это безопасно!
Метаанализ за 15 лет показал полную безопасность с незначительными редкими побочными эффектами. 62 рандомизированных клинических испытания, в которых приняли участие 3546 участников с диагнозом различных заболеваний (около 20 видов заболеваний), получавших внутривенную или местную имплантацию по сравнению с плацебо или отсутствием лечения. Все исследования были высокого качества, и во включенных исследованиях не было обнаружено ни серьезной систематической ошибки публикации, ни серьезных нежелательных явлений (таких как смерть и инфекция). Объединенный анализ показал, что введение МСК было тесно связано с транзиторной лихорадкой р < 0,01), побочными эффектами в месте введения (р = 0,05). , запор (р = 0,05), утомляемость (0,04) и бессонница (р = 0,05). Интересно, что введение МСК имело тенденцию к снижению, а не увеличению частоты возникновения аритмии ( р = 0,09). Выводы. Убедительно, что введение МСК было безопасным в различных популяциях по сравнению с другими методами плацебо. pubmed.ncbi.nlm.nih.gov/34663461/
Но, надо понимать, что сам по себе диагноз СД 1 типа многократно повышает риск онкозаболеваний, поэтому чем раньше вы обратитесь с момента манифестации, тем ниже любые риски.
КЛИНИЧЕСКАЯ ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ПРИ САХАРНОМ ДИАБЕТЕ
Этот метаанализ показал, что терапия МСК может быть эффективным и безопасным вмешательством у пациентов с диабетом. (pubmed.ncbi.nlm.nih.gov/33705413/)
Клеточная терапия при сахарном диабете 1 типа направлена на решение двух важных задач:
- репрограммирование клеток иммунной системы для предотвращения разрушительного действия на В-клетки;
- восстановление/создание общего пула дееспособных В-клеток;
- предупреждение и снижение системного стерильного воспаления.
Клеточные технологии применяемые для терапии СД 1 типа существуют разные. Применяют как аутологичные (собственные) стволовые клетки, так и донорские. Кроме того могут использоваться персонифицированные клеточные препараты из компонентов крови (экзосомы).
По источнику происхождения стволовые клетки
Могут быть мобилизованы ГСК (гемопоэтические стволовые клетки) из периферической крови. На видео ниже автору метода терапии сахарного диабета 1 типа (Патент РФ) Захарову Ю.А., проводится мобилизация ГСК для последующей трансплантации. Мобилизованные таким образом стволовые клетки могут быть в дальнейшем модифицированы или не модифицированы для трансплантации.
Отработанная, в том числе и на детях, в течение более 20-ти лет лицензированная процедура с утвержденным безопасным протоколом мобилизации аутологичных (собственных) гемопоэтических стволовых клеток до сих пор использовалась в основном в онкогематологии.
Ситуацию изменило клиническое исследование NCT00315133 (Comite de Ética em Pesquisa do HCFMRP-USP, No 10095/2002), когда процедура введения неизмененных ГСК вызвала у пациентов с СД 1 типа длительную ремиссию без инсулинотерапии (www.frontiersin.org/articles/10.3389/fimmu.2017.00167/full)
Это получило дальнейшее развитие в экспериментальных программах проводимых совместно клиникой “Нейровита” (РФ) и Канадским институтом регенеративной медицины (Онтарио).
К сожалению, пациенты часто переоценивают, как показывает недавнее исследование: www.nature.com/articles/s41536-022-00215-w, возможности клеточной терапии. В тоже время, недооценивая комбинированную терапию (иммунотерапия), что приводит к аналогичным результатам. Кроме того, клеточная терапия стволовыми клетками требует длительного дополнительного наблюдения и сопровождения.
В России (Москва) начаты клинические испытания по программе: “Поддержка иммунного ответа ГСК” (программы аналогичная выше указанному исследованию, технически проводится см. видео с автором метода терапии СД 1 типа», профессором кафедры экспериментальной медицины Канадского института регенеративной медицины Захаровым Ю.А.

После проведения клеточной терапии вы получите сертификат (клеточный паспорт) лаборатории, которая создала клеточный препарат или работала над вашими клетками (пример лаборатории, которая ранее работала с нами до 2023 г.:



МСК мобилизованные из жировой ткани использовались нами ранее см. видео, но в настоящее время применяется более современная технология:
Аутологичная трансплантация гемопоэтических стволовых клеток (AHSCT) увеличивает уровни C-пептида и индуцирует инсулинонезависимость у пациентов с диабетом 1 типа. (www.frontiersin.org/articles/10.3389/fimmu.2017.00167/full)
Пациенты с первичным СД1 были успешно возвращены к нормогликемии с помощью аутологичной немиелоаблативной трансплантации гемопоэтических СК. Наконец, эмбриональные СК также открывают захватывающие перспективы, поскольку они способны генерировать чувствительные к глюкозе клетки, продуцирующие инсулин. (pubmed.ncbi.nlm.nih.gov/21862682/)
МСК могут регулировать субпопуляции Т-клеток для восстановления их иммунного гомеостаза в направлении разрешения болезни при аутоиммунных состояниях. (pubmed.ncbi.nlm.nih.gov/33859701/)
В новом исследовании показан потенциал как предшественников поджелудочной железы, полученных из стволовых клеток, так и более зрелых продуцирующих инсулин клеток для лечения диабета, оптимизация параметров биопроцесса с целью облегчения масштабируемого производства эндокринных клеток поджелудочной железы, полученных из плюрипотентных стволовых клеток человека (stemcellsjournals.onlinelibrary.wiley.com/doi/10.1002/sctm.21-0161).
У некоторых пациентов уровни С-пептида сохранялись на одном уровне до 2 и более лет после однократного введения клеток. (www.ncbi.nlm.nih.gov/pmc/articles/PMC4729454/).
Внутривенное введение мезенхимальных стволовых клеток (МСК) подавляет аутоиммунные заболевания, в том числе и СД 1 типа. (clinicaltrials.gov/ct2/show/NCT04061746).
Терапия стволовыми клетками достигла наиболее перспективных результатов в сравнении с применением стандартных иммунодепрессантов. (www.ncbi.nlm.nih.gov/pubmed/28260183).













ПРИМЕЧАНИЕ: Видеоизображения (интервью), ссылки на научные публикации размещены на сайте для СПЕЦИАЛИСТОВ и не предназначены для пациентов, во избежание необоснованной мотивации к использованию подобных технологий. Имеются строгие показания и противопоказания. Обязательна консультация с лечащим врачом и проведение межклинического консилиума. Здесь представлена информация для специалистов, информация для пациентов в разделе: «Запись на прием». Гарантии предоставляются только на качество медицинских процедур выполняемые в условиях стационара/дневного стационара в рамках лицензии на право медицинской деятельности.
Подробнее в книгах (пять томов) профессора кафедры экспериментальной медицины Канадского института регенеративной медицины (Торонто, Онтарио) Юрия Захарова:
